Nombre de traitements pour certaines maladies nécessitent un suivi rapproché afin que soit évalué le dosage médicamenteux. Alors que la population québécoise est vieillissante, ces suivis engorgent les cliniques et les laboratoires. Environ 200 000 Québécois ont ce besoin en raison d’une insuffisance cardiaque. Or, le développement de tests rapides, peu coûteux et simples pour la détection quantitative des biomarqueurs dans le sang aurait un effet considérable sur la santé des individus en favorisant le diagnostic, la surveillance et le traitement à domicile de maladies. Un groupe de recherche en bionanotechnologies de l’Université de Montréal travaille actuellement à développer un outil diagnostique portatif qui permettra de suivre l’évolution de l’insuffisance cardiaque avec une seule goutte de sang : le biosenseur.
Selon la courbe démographique, la proportion de personnes âgées est croissante depuis 2011 au Québec[1], et la proportion de Québécois âgés de 65 ans et plus a même doublé de 1981 à 2016. Cette évolution démographique vient avec son lot de défis et l’augmentation de l’âge moyen de la société affecte nécessairement le système de santé. Ce changement démographique influe particulièrement sur le nombre d’individus souffrant d’insuffisance cardiaque, car la prévalence de développer cette maladie après 55 ans est de 30 %[2]. Ainsi, au Canada en 2016, 600 000 personnes souffraient de cette maladie, qui était responsable de 9 % des décès pour la même année[3]. Corrélativement au vieillissement de la population, la prévalence des maladies chroniques et les coûts des soins de santé connexes ont grimpé en flèche, ce qui rend difficile l’amélioration de la qualité et de la portée des soins de santé pour ceux qui en ont besoin. Une solution prometteuse est de déplacer les soins de santé des hôpitaux et des laboratoires centralisés vers de petites cliniques et au domicile des patients grâce aux biosenseurs. Ces derniers sont des engins qui utilisent de la matière biologique tel le sang pour détecter la concentration d’une substance dans le corps.
Un traitement imparfait
Abonnez-vous à notre infolettre!
Pour ne rien rater de l'actualité scientifique et tout savoir sur nos efforts pour lutter contre les fausses nouvelles et la désinformation!
L’insuffisance cardiaque est un problème de santé où le cœur ne parvient pas à pomper et à faire circuler un approvisionnement adéquat en sang pour répondre aux exigences du corps. Les muscles du cœur deviennent endommagés et moins efficaces, ce qui entraîne une surcharge sur le cœur. Certaines maladies nécessitent des traitements qui peuvent avoir des effets néfastes sur d’autres organes. C’est notamment le cas de l’insuffisance cardiaque, qui peut être traitée avec une classe de médicaments, les inhibiteurs de l’enzyme de conversion de l’angiotensine (ECA)*[4].Ces médicaments agissent sur le cœur en ouvrant les vaisseaux sanguins et en diminuant la pression artérielle, ce qui facilite l’action de pompage du cœur. Toutefois, ils abaissent également le débit de filtration des reins. Un usage prolongé de ces médicaments peut donc s’avérer potentiellement toxique pour les reins[5] et mener à une insuffisance rénale aiguë*, même chez les patients présentant au début du traitement une fonction rénale normale.
Ainsi, pour contourner ce problème, des doses sous-optimales du médicament sont prescrites aux patients, ce qui leur permet de contrôler et d’atténuer le problème initial d’insuffisance cardiaque, sans que des complications aux reins soient pour autant créées. Toutefois, cette limitation thérapeutique a aussi ses inconvénients, car en plus de restreindre l’action du médicament sur l’insuffisance cardiaque, elle oblige les patients à subir des prélèvements sanguins à répétition afin de suivre l’effet de la médication et de trouver la dose appropriée tout en s’assurant que les reins ne sont pas touchés. Trois marqueurs sanguins indicatifs à la fois de l’état cardiaque et de celui des reins sont généralement mesurés et observés : le potassium, la créatinine et l’urée[6]. Une concentration trop élevée de ceux-ci indique un déséquilibre et peut signifier une détérioration de la santé de l’individu.
Les trois composantes
Au cours de la dernière décennie, d’importants efforts ont permis de faire du progrès dans le développement des technologies permettant des tests diagnostiques plus simples à effectuer et à un moindre coût : les biosenseurs. Ceux-ci se basent sur le principe des glucomètres, qui utilisent une petite quantité de sang pour détecter la concentration de glucose sanguin. Les glucomètres portatifs illustrent bien les avantages de ces technologies, qui aident des millions de patients diabétiques à surveiller leur niveau de glucose et à traiter leur diabète dans leur maison. Au Laboratoire de biosenseurs et nanomachines de l’Université de Montréal, les recherches s’orientent autour des trois marqueurs sanguins principaux, soit le potassium, la créatine et l’urée. L’objectif est de développer des biosenseurs à base d’ADN* pour détecter ces biomarqueurs sanguins. Dans les prochaines années, les patients atteints d’insuffisance cardiaque pourront effectuer leurs prélèvements sanguins de leur domicile grâce à cette technologie.
Différents groupes de recherche travaillent sur le développement des biosenseurs. Chaque famille de biosenseurs a un mode de fonctionnement qui lui est propre, mais pour être fonctionnel, l’appareil doit généralement contenir trois composants distincts. Premièrement, une surface conductrice, comme une électrode d’or*, est nécessaire comme support physique de l’architecture du biosenseur. Deuxièmement, un élément spécifique, l’ADN dans ce cas-ci, capable de reconnaître les marqueurs sanguins est requis. Finalement, le biosenseur a besoin d’un élément de signalisation sensible et quantifiable qui communique avec la surface conductrice. Cet élément est une molécule électro-active*, comme la molécule de bleu de méthylène. La combinaison de l’ADN sous forme d’aptamère* et de l’électrochimie sur une électrode d’or pour la détection précise et performante des marqueurs sanguins est une voie prometteuse. La combinaison de ces principes dans un biosenseur produit une technologie hautement ciblée et sensible.
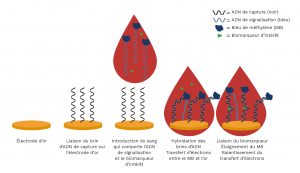
La base du biosenseur est l’électrode d’or, sur laquelle les autres composants sont ajoutés (figure 1). Tout le système fonctionne à partir de cette électrode d’or miniature de moins de 1 cm2. La surface d’or est branchée à un circuit électrique qui envoie un courant électrique et qui mesure les échanges à la surface d’or. Ce métal convient parfaitement, car il ne réagit pas avec les autres molécules et a une grande conductivité de l’électricité[7]. La surface d’or reçoit le deuxième matériau du biosenseur, l’ADN. Ce dernier représente la base du code génétique ; il est composé de quatre bases différentes (adénine, thymine, guanine et cytosine) qui se lient selon un appariement rigoureux[8]. Une séquence de ces bases forme un brin d’ADN. La liaison entre deux brins d’ADN est appelée « hybridation » ; c’est elle qui crée la structure de double hélice.
Figure 1. Le processus de préparation et de fonctionnement du biosenseur
Une découverte significative dans le domaine de l’ingénierie moléculaire est la conception de séquences d’ADN synthétique nommées « aptamères ». Les aptamères présentent de nombreux avantages en tant qu’éléments de reconnaissance dans le biosenseur par rapport aux autres méthodes de détection traditionnelles. Ces séquences sont potentiellement capables de reconnaître par appariement tout type de molécule, des lipides aux protéines, en passant même par les hormones. Elles ont la caractéristique unique d’être très spécifiques et sélectives. Elles sont ainsi à la base du biosenseur : un aptamère peut être conçu directement pour cibler une composante sanguine telle que la créatinine pour l’insuffisance cardiaque et la reconnaître ensuite dans le sang[9].
Alors que l’ADN permet la spécificité du biosenseur, un autre domaine scientifique est essentiel pour la signalisation entre la surface d’or et l’ADN : l’électrochimie. Il s’agit de la relation entre l’électricité et les changements mesurables et quantifiables sur le plan chimique. Cette branche de la chimie mesure et observe les transferts d’électrons, qui sont quantifiables, d’une molécule à une autre en présence d’un circuit électrique[10]. L’électrochimie est donc le mode de communication entre l’ADN et la surface d’or. Elle permet de mesurer l’hybridation de l’ADN et donc de détecter la concentration des biomarqueurs d’intérêt. Certaines molécules électro-actives sont plus aptes à transférer des électrons à cause de leur disposition tridimensionnelle. Plus la molécule électro-active est proche de la surface, plus le transfert d’électrons sera important et rapide. Si la molécule est éloignée de la surface, le rythme d’échange sera plus lent et moindre. Le bleu de méthylène est la molécule électro-active employée dans la famille de senseurs développés à l’Université de Montréal.
Une fermeture éclair moléculaire
Pour utiliser le biosenseur, la personne dépose une goutte de sang du bout de son doigt sur le détecteur. Le sang voyage dans l’instrument et se mélange avec de l’ADN avant de se déposer sur la surface d’or. Là, une combinaison de réactions chimiques se produit et avec l’aide d’algorithmes et de programmes informatiques, l’information contenue dans la goutte de sang est transformée en une donnée de concentration sanguine. Cette concentration est affichée sur le biosenseur pour le patient et est envoyée au médecin.
La fermeture éclair permet une analogie avec le système de détection de ce biosenseur. Chaque fermeture éclair est spécifique à un habit. Elle est composée de deux bandes de dents métalliques complémentaires, mais différentes : une contient le curseur tandis que l’autre, non. L’aptamère d’ADN peut être vu comme une fermeture éclair : chaque bande de dents métalliques d’une fermeture éclair représente un brin d’ADN. Comme une fermeture éclair qui est choisie pour un vêtement en particulier, un aptamère est sélectionné pour sa spécificité à une cible moléculaire et deux brins distincts sont synthétisés : un brin pour se lier à la surface d’or et un brin qui comporte la molécule électro-active à l’une de ses extrémités. Lorsque les deux parties de dents métalliques s’emboîtent, la fermeture éclair s’unit et crée un objet. C’est la même chose pour l’aptamère : quand les deux brins d’ADN sont mis en contact, ils s’unissent et créent une seule structure d’ADN. Quand la fermeture est liée, le curseur se retrouve en haut. Dans un biosenseur, le curseur est représenté par la molécule électro-active, qui communique avec le bas de la fermeture. Bouger la fermeture éclair fermée va changer sa disposition et l’emplacement de ses éléments. Avec le biosenseur, l’introduction du sang correspond à ce mouvement. Le biomarqueur d’intérêt (comme l’urée ou la créatinine) va changer la disposition du système de « fermeture éclair » en se liant à l’aptamère et va faire s’éloigner le curseur du bas de la fermeture. Ce déplacement du curseur est proportionnel à la quantité du biomarqueur et la concentration de celui-ci peut ainsi être calculée. Elle devient alors une donnée utilisable par le médecin. Les biosenseurs surveillent et étudient cette variation de transfert ; celui-ci étant quantifiable, en connaître la variation permet de déduire la concentration du biomarqueur dans le sang.
Un potentiel immense
Actuellement, cette recherche est développée en laboratoire à petite échelle. Une fois ce senseur terminé, les étapes de préparation des électrodes seront faites à l’avance. Le patient souffrant d’insuffisance cardiaque pourra alors recevoir les électrodes directement à son domicile et utiliser simplement cette technologie en déposant une goutte de sang sur le détecteur. L’accessibilité de ces tests sanguins sera l’avantage principal de cet engin. Le biosenseur permettra aux médecins de prescrire les doses optimales des médicaments pour traiter cette pathologie, car ils pourront suivre en temps réel leurs effets toxiques sur les autres organes. Dès que des irrégularités comme des concentrations sanguines trop élevées se manifesteront, les médecins recevront l’information et pourront ajuster rapidement les doses de médicaments pour un traitement optimal. De plus, cette nouvelle technologie de biosenseurs se développe aujourd’hui pour le suivi de l’insuffisance cardiaque, mais sa méthodologie pourrait être transposée à une multitude d’autres maladies par la détection d’un nombre quasi infini de molécules dans le sang. Pour la société, cela représentera un désengorgement des hôpitaux, un meilleur accès aux soins et aussi une atténuation des coûts liés à la santé. Bien que les biosenseurs ne soient que de petits engins, leur portée peut devenir immense.