Si je vous dis comme ça qu’on vient de réussir à enregistrer simultanément l’activité de 12 000 neurones dans le cortex de souris libres de leurs mouvements avec une résolution à l’échelle cellulaire et jusqu’à 17 Hertz de fréquence, vous me répondez quoi ? Quelque chose comme « Et alors ? », « Je m’en fous » ou « Peux-tu me parler pour que je te comprenne ? ». C’est le défi de cette dernière réponse que je vais tenter de relever dans le reste de ce billet. Parce que si je réussis, votre réponse deviendra sans doute semblable à la mienne, à savoir un écarquillement des yeux accompagné de quelques « incroyable !, fabuleux !, malaaade ! » bien appuyés. Mais pour ça, il faut d’abord faire quelques pas en arrière…
Le cerveau humain, qu’on aimerait bien comprendre un peu mieux, est très très très complexe. Il possède environ 86 milliards de neurones, autant de cellules gliales, et l’enchevêtrement des dendrites et axones de ces neurones est tel que l’on pourrait, si on les sortait d’un seul cerveau et on les mettait bout à bout, faire environ quatre fois le tour de la Terre ! C’est pour ça qu’on se rabat souvent sur le cerveau de rat ou de souris, gros comme le bout de notre petit doigt, pour essayer de comprendre la dynamique complexe des influx nerveux qui voyagent dans cette forêt de neurones. Parce que c’est ça aussi le problème : il ne s’agit pas seulement de comprendre l’inextricable connectivité des neurones, il faut surtout comprendre comment l’influx nerveux y circule, quels neurones sont activés à un temps donnés, lesquels sont silencieux ou activés en même temps à ce moment-là, etc.
Au milieu du XXe siècle, on a découvert qu’avec de toutes petites électrodes en verre ou en métal, on pouvait enregistrer l’activité électrique des neurones soit en enfonçant l’électrode dans un neurone, soit en restant à l’extérieur près d’un petit groupe de neurones. Ces enregistrements intra ou extracellulaires amènent, vous vous en doutez bien, leur lot de problèmes et de contraintes techniques. Il y a tout ce qu’on risque d’abimer avec notre électrode, y compris la cellule qu’on veut enregistrer. Il y a aussi le petit nombre de cellules qu’on peut enregistrer en même temps, le manque de précision sur la provenance des signaux quand on enregistre en extracellulaire, etc.
Abonnez-vous à notre infolettre!
Pour ne rien rater de l'actualité scientifique et tout savoir sur nos efforts pour lutter contre les fausses nouvelles et la désinformation!
Sur une note personnelle, je me souviens de ces longues heures passées durant deux ans à approcher des neurones d’Aplysie avec de telles électrodes. Et le plaisir éprouvé quand je parvenais à mettre en évidence une connexion entre un neurone sensoriel et un neurone moteur de ce mollusque marin. Le petit hic, c’est que même un invertébré comme l’Aplysie avait tout de même 20 000 neurones et que moi je ne pouvais en entendre que deux à la fois « se parler ». Que disaient tous les autres pendant ce temps-là ? On me pouvait pas le savoir.
On était alors au début des années 1990 et depuis une décennie et dans la décennie qui allait suivre se développait en parallèle une autre approche permettant celle-là de « visualiser » directement l’activité des cellules nerveuses : l’imagerie au calcium. Le calcium est un ion (Ca2+) qui entre naturellement dans un neurone quand celui-ci est excité par d’autres neurones, ce qui l’amène à produire des influx nerveux. En fait, c’est évidemment plus compliqué que ça, le calcium pouvant aussi être libéré de l’intérieur même de la cellule par toutes sortes de compartiments. Mais en gros sa concentration interne peut être multipliée par 10 ou même par 100 à certains endroits dans le neurone quand celui-ci reçoit des excitations d’autres neurones, ce qui permet alors aussi aux mécanismes de plasticité synaptique de se mettre en marche. Or dans les années 1980 et 1990, on a commencé à développer deux outils qui vont nous permettre de comprendre l’exploit dont je veux vous parler aujourd’hui.
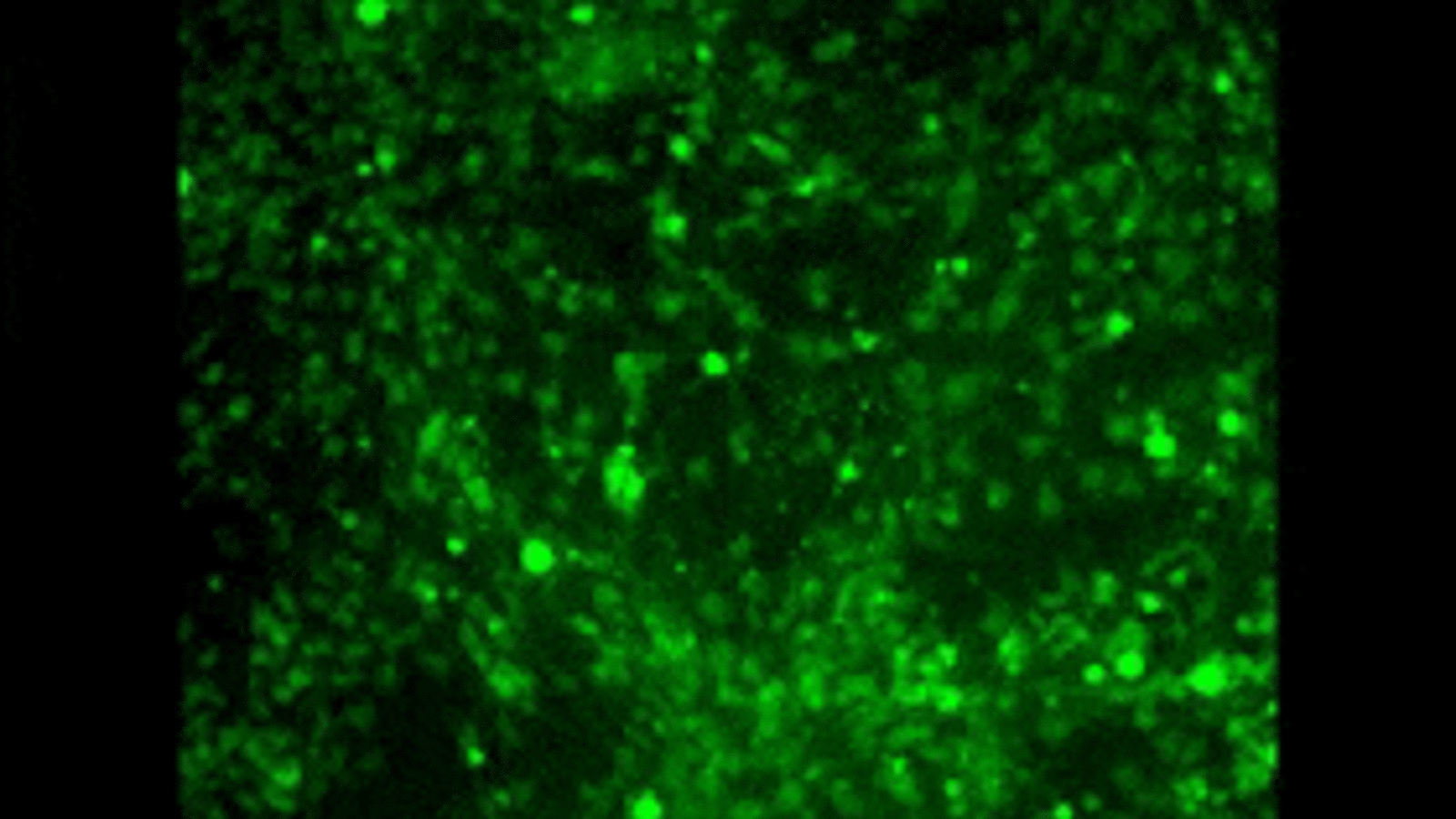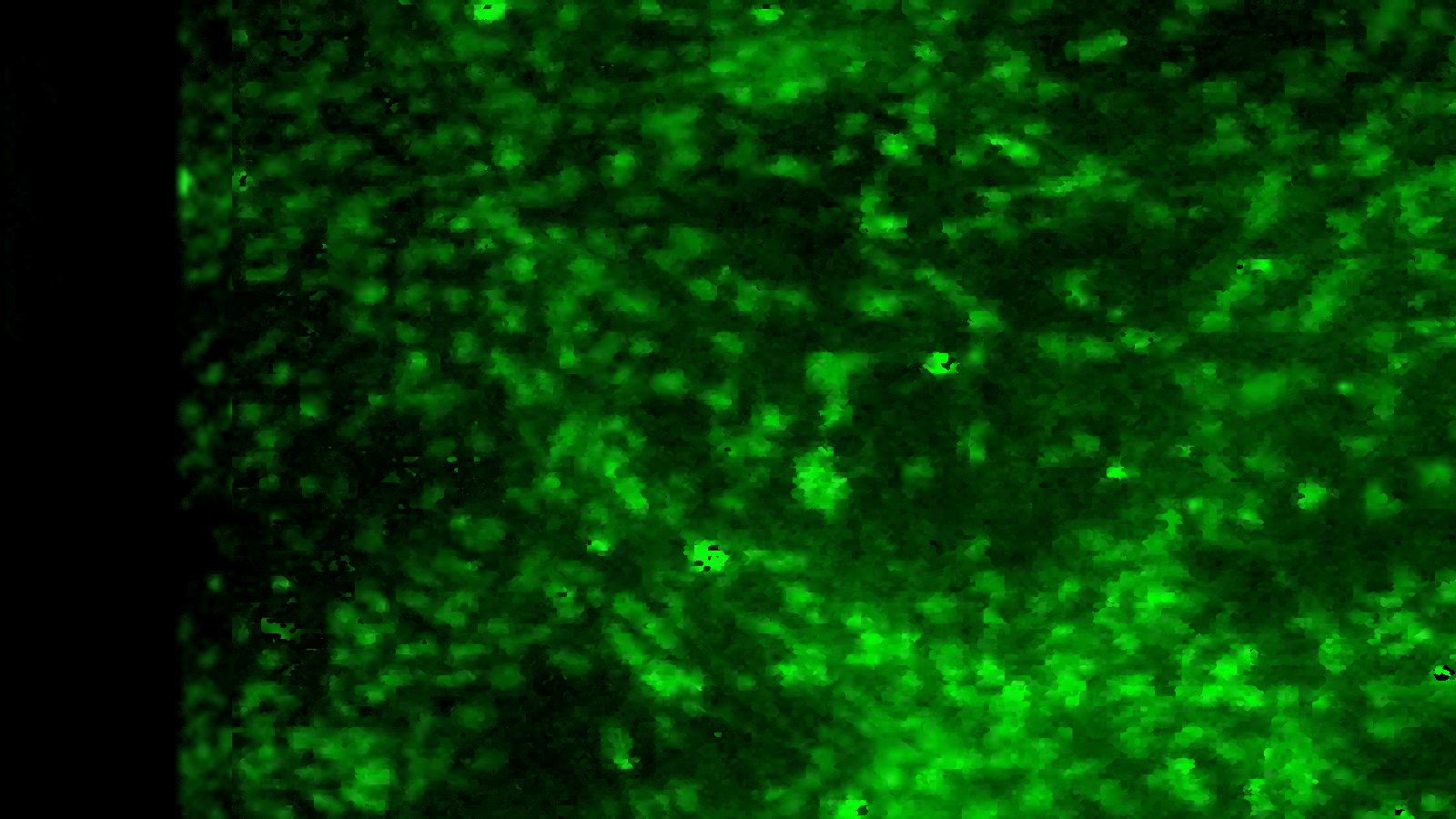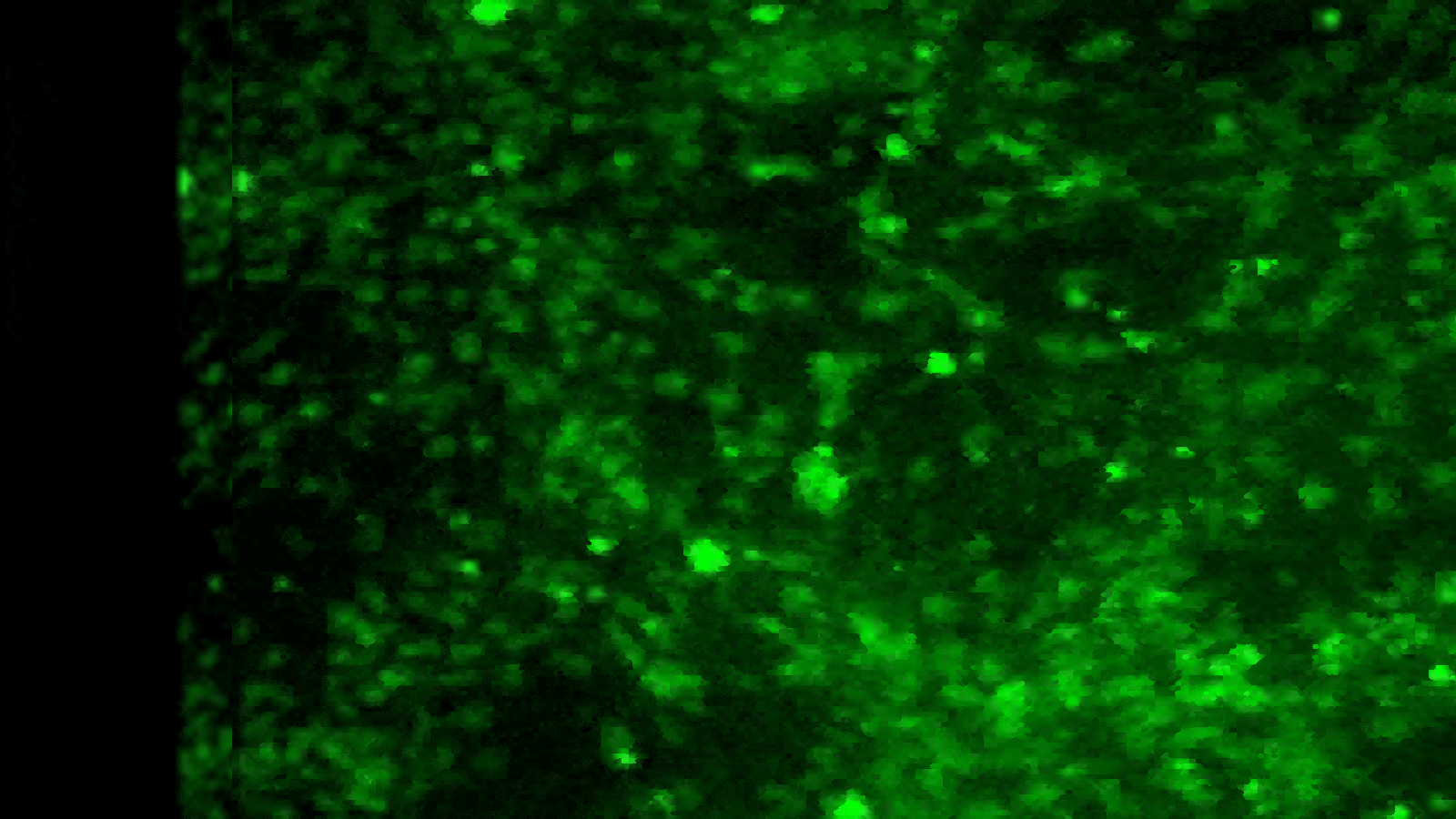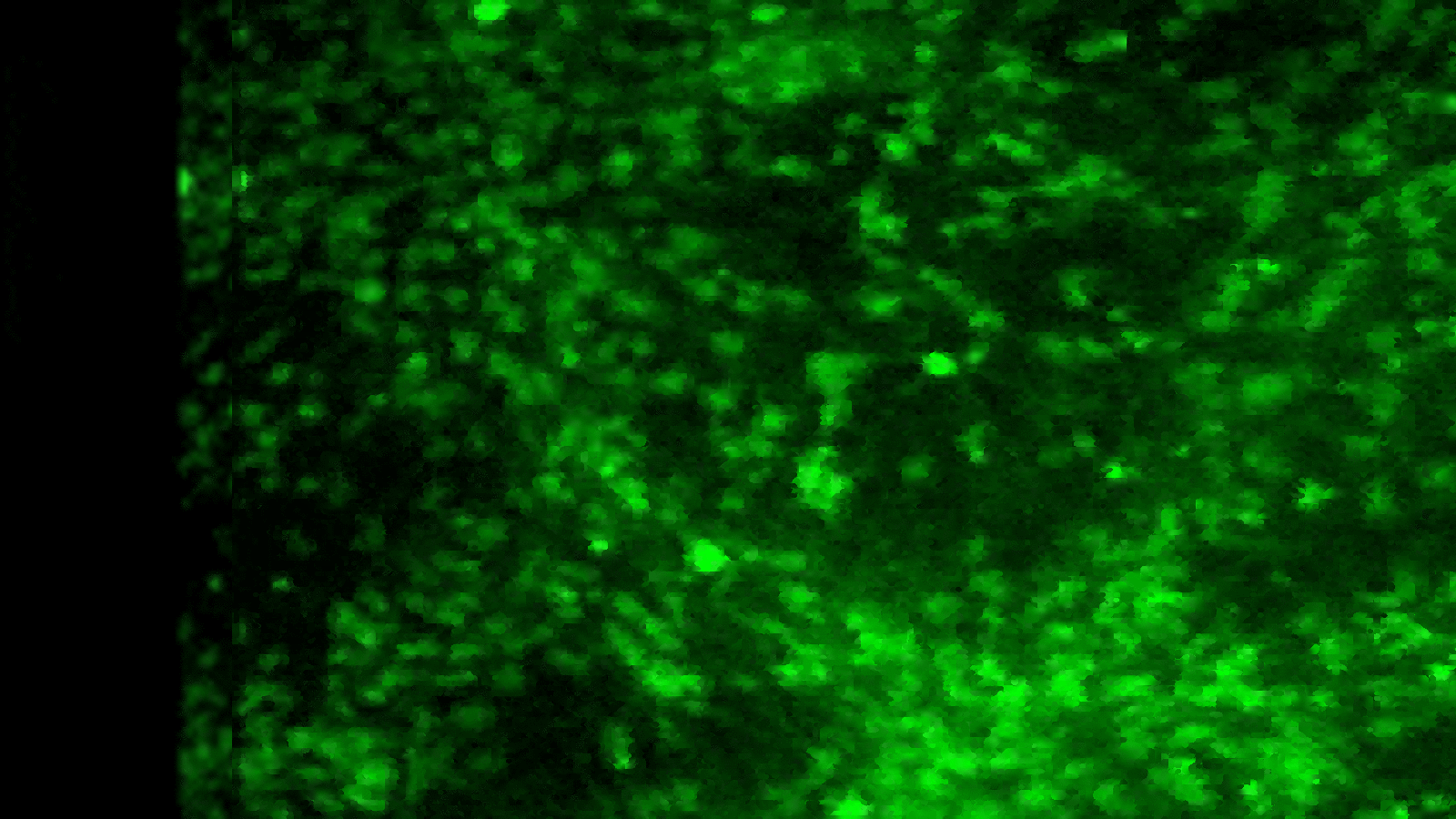
D’abord des molécules fluorescentes dont la fluorescence change selon la concentration de calcium du milieu dans lequel elles se trouvent. Je n’entrerai pas dans la nature des diverses molécules qui peuvent avoir cette propriétés, sinon pour souligner qu’un des problèmes associés est de trouver comment les faire rentrer dans de grandes populations de cellules en même temps. Car vous me voyez peut-être venir : ce sera l’une des forces de l’imagerie au calcium que de permettre de visualiser l’activité d’innombrables neurones en même temps (voir l'image en haut de ce billet qui n'est cependant pas tirée de l'étude présentée ici). Et comme vous vous en doutez bien aussi, on a effectivement réussi à trouver comment les faire passer à travers les membranes cellulaires ou même comment les faire fabriquer par les cellules elles-mêmes suite à des manipulations génétiques.
L’autre domaine qui a nécessité des développements techniques importants fut celui des techniques de microscopie permettant de visualiser en temps réel ces fluctuations d’ions calcium qui correspondent à de l’activité nerveuse. Je vous passe tous les noms compliqués de ces techniques, de la microscopie confocale aux caméras vidéo CCD, pour vous parler de l’une des plus puissantes : la microscopie à deux photons. À la différence de la microscopie confocale ordinaire qui utilise un faisceau laser à un photon pour exciter la molécule fluorescente au calcium, comme son nom l’indique le microscope à deux photons en envoie deux. Sauf que chacun a un niveau d’énergie inférieur à ce qui est nécessaire pour activer la molécule fluorescente. Mais leur interférence à des endroits spécifiques amène la sommation de leur énergie et permet alors d’exciter suffisamment les molécules fluorescentes pour qu’elles émettent leur lumière.
Plusieurs avantages découlent de cette approche dont la moins grande toxicité des rayons laser pour les cellules. Mais surtout, la possibilité d’enregistrer plusieurs centaines de microns en profondeur dans le cortex à partir de sa surface. On a même inventé des espèces de casques miniatures que peut porter une souris en se promenant dans sa cage pendant que ce microscope à deux photons miniature enregistre les flux de calcium de ses neurones corticaux jusque dans ses moindres épines dendritiques !
Mais pour en revenir à l’étude dont je voulais vous parler et qui vient d’être publiée le mois dernier dans la revue Cell, elle a pour titre : « Volumetric Ca2+ Imaging in the Mouse Brain Using Hybrid Multiplexed Sculpted Light Microscopy ». Et elle a permis, comme je le disais en introduction, d’enregistrer près de 12 000 neurones en même temps dans un volume de 1mm x 1mm x 1,22 mm dans différentes régions du cortex d’une souris pendant que celle-ci vaquait tranquillement à ses occupations. Si maintenant la mâchoire ne vous décroche pas un peu de stupéfaction, je ne sais pas ce qui pourra le faire !