Explication. En temps normal, dans la nature, un virus ne se propage qu’entre membres d’une même espèce. Un «virus d’oiseaux» qui se transmet à un mammifère, c’est censé être une mutation exceptionnelle. Ce même virus qui subirait une seconde mutation, le rendant capable de se transmettre d’un mammifère à un autre mammifère, ce serait encore plus exceptionnel —et du coup, très inquiétant pour l’humain.
Abonnez-vous à notre infolettre!
Pour ne rien rater de l'actualité scientifique et tout savoir sur nos efforts pour lutter contre les fausses nouvelles et la désinformation!
Or, c’est exactement ce que deux équipes distinctes, une aux Pays-Bas et une aux États-Unis, avaient annoncé à l’automne 2011: en laboratoire, avec seulement quelques manipulations génétiques, ces chercheurs étaient parvenus à obtenir une souche de la grippe aviaire —le H5N1— soudain capable de se transmettre entre des furets —donc, des mammifères, comme nous. La nouvelle avait provoqué une telle émotion que le 20 décembre 2011, après bien des discussions de coulisses, il avait été décidé que les articles seraient publiés, mais que les données les plus «sensibles» seraient mises sur la glace jusqu’à nouvel ordre. Ce n’est qu’en mai 2012 qu’il était finalement décidé qu’il ne servait à rien de ne pas publier la totalité des données.
Depuis le 31 mars 2013, on sait que, quelque part en Chine, le H7N9 a franchi la première étape: une mutation qui lui permet de se transmettre d’oiseaux à mammifères —en l’occurrence, nous. Une hypothèse, non vérifiée, veut qu’il ait d’abord transité par les porcs.
Ce que tout le monde craint à présent, c’est une seconde mutation, qui lui permettrait de se transmettre d’humain à humain. Le 8 avril, l’Organisation mondiale de la santé (OMS) se voulait rassurante: une telle mutation, affirme-t-elle, ne s’est pas encore produite.
Si le H7N9 s’avère transmissible entre humains, avons-nous une parade?
Pas pour l’instant. Les vaccins contre la grippe couvrent «nos» versions du virus, qui sont des cousins trop éloignés d’une grippe aviaire.
Est-ce déjà arrivé?
Le H5N1 était un exemple de grippe aviaire transmise aux humains de façon très virulente: 360 morts dans le monde, sur environ 600 cas, soit plus de la moitié, étalés entre 2003 et 2013 (le virus court toujours). C’est cette virulence du H5N1 qui a fait craindre le pire lorsqu’a surgi, au Mexique en 2009, le H1N1, alors appelé grippe porcine —lequel s’est, au final, avéré moins dangereux.
Pourquoi le H7N9 correspondrait-il au scénario inquiétant?
Personne ne peut répondre à cette question pour l'instant. Tout nouveau virus de ce type est potentiellement inquiétant, à cause des mutations possibles. L’alerte provient aussi du fait que les trois premiers cas humains recensés en Chine n’étaient pas liés entre eux, ce qui suggère qu’ils l’ont chacun attrapé d’un animal différent —donc, que le virus voyage déjà depuis un bout de temps.
D’un autre côté, quatre des six premiers décès sont à Shanghaï, mégalopole du sud de la Chine, où des abattages massifs d’oiseaux et de volailles ont été décrétés les 5 et 6 avril.
Le scénario du pire, c’est la transmission entre humains et un haut pourcentage de cas virulents, voire de décès. Quel est le scénario optimiste?
Une grande majorité de cas bénins —dont beaucoup de gens qui n’ont même pas su qu’ils souffraient d’une grippe différente de la normale— et une minorité de cas très sévères. C’est le scénario habituel d’une pandémie de grippe, aviaire ou non. Le virus pourrait aussi faire parler de lui pendant quelques mois, puis se faire oublier dans la nature —c’est ce qui s’était produit avec le H5N1, apparu à Hong Kong en 1997, puis réapparu à la fin de 2003.
La Chine est-elle équipée pour y faire face?
Oui. Elle a été critiquée pour sa lenteur à réagir —les deux premiers cas ont été rapportés à la fin de février, et les deux premiers décès ont eu lieu les 4 et 10 mars. Mais dès la première annonce publique du 31 mars, l’agence nationale de santé a commencé à diffuser les analyses génétiques du virus. Les données sont partagées au fur et à mesure, entre autres sur un serveur européen de l’OMS, accessible à tous les chercheurs du monde. Déjà, ces analyses ont fourni des pistes quant à l’origine du virus.
Qui plus est, les autorités chinoises montrent depuis le début d’avril une volonté de diffuser et de partager l’information qu’on leur connaissait peu. [ Ajout 12 avril: La première étude sur les trois premiers patients décédés, offre des malades un portrait sombre ]
Mais ces choses-là prennent du temps, et il y aura d’autres morts. Lorsqu’une personne se présente à l’hôpital avec une pneumonie, il peut s’écouler du temps avant qu’on ne fasse des tests pour identifier la cause, et d’autres malades ont fort probablement échappé aux écrans radar.
Ce virus ne comporte que huit gènes. Depuis le 31 mars, il a déjà été établi que ces huit gènes sont propres à la famille aviaire de la grippe. Mais ils montrent aussi des signes qui, pour les experts, trahissent le fait qu’ils se sont adaptés à un hôte différent, un mammifère: porc, humain, ou les deux? Ça reste à découvrir. [Ajout 10 avril: pour découvrir la source du virus, les scientifiques travaillent sur plusieurs fronts à la fois. ]
Ces mutations signifient que le virus peut désormais s’accrocher aux cellules des voies respiratoires de son hôte: c’est traditionnellement ainsi qu’une bonne grippe nous infecte.
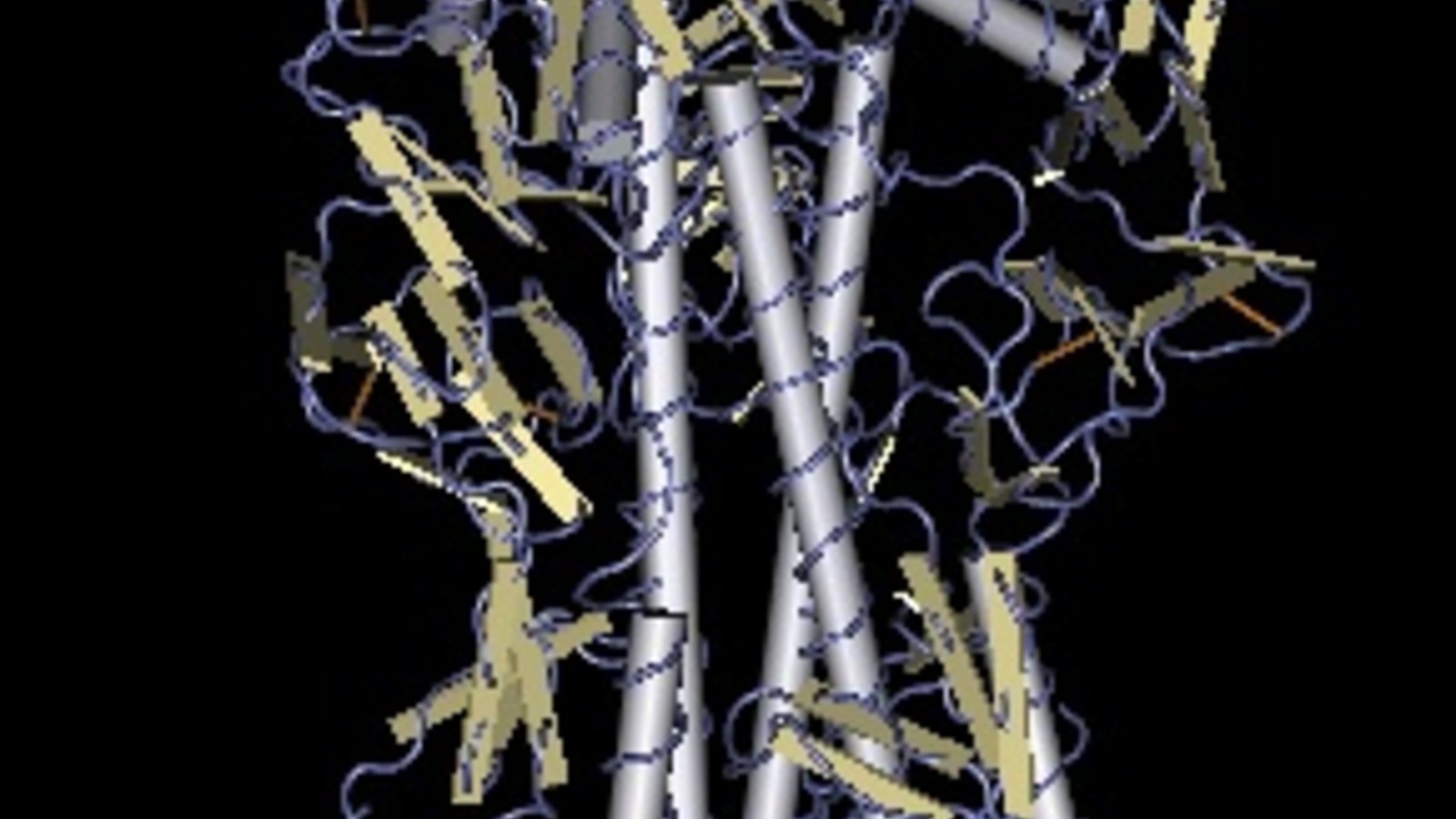
Deux de ces gènes encodent les protéines H et N qui donnent son nom, H7N9, au virus: l’hémagglutinine et la neuraminidase. Parce qu’elles sont logées à la surface du virus, ce sont ces protéines qui permettent au virus de s’accrocher —ou non— à sa cible. Une mutation-clef (il n’y en a sûrement pas qu'une seule) pourrait donc se cacher là.
C’est parce que ce type de question est complexe qu’il a été établi en 2011-2012 que les données des recherches controversées mentionnées plus haut, devaient être accessibles à tous: parce que plus les experts en virus ont accès aux données sur un maximum de variétés d’un virus, plus ils augmentent leurs chances de trouver une parade à cette variété-ci.